Химическая промышленность: состав, факторы размещения, основные районы и центры. Проблемы и перспективы развития. Химическая промышленность и окружающая среда. и зачем ее изучать? Соли азотной кислоты
Химическая система - сочетание веществ, взаимодействующих друг с другом. Система отделяется от окружения мысленно или фактически. Химические системы делятся на следующие виды:
а) гомогенные
б) гетерогенные
в) дисперсионные
г) нонвариантные
д) моновариантные
е) бивариантные
ж) поливариантные.
Гомогенная система - физико-химическая система, содержащая одну фазу.
В гомогенной системе, включающей два и более химических компонента, каждый из компонентов распределяется в объеме другого соединения в виде молекул, атомов или ионов. Компоненты гомогенной системы имеют определенные значения по системе или непрерывно меняющиеся от одной к другой точке системы. Известны следующие гомогенные системы: лед, жидкие или твердые растворы, смеси газов. При этом различают жидкие, кристаллические и аморфные вещества.
Гетерогенная система - система, включающая несколько гомогенных частей (фаз), разделенных границами.
Фазы могут отличаться одна от другой составом и свойствами.
Фаза - гомогенная часть гетерогенной системы, имеющая одинаковые свойства во всех точках и отделяющаяся от других частей границами.
Дисперсная система - система мельчайших частиц (твердых, жидких или газообразных), суспендированных в жидкой, газообразной или твердой среде (дисперсная среда).
Примерами дисперсных систем являются: молоко, в котором частицы жира суспендированы в воде, а также различные эмульсии, суспензии, туманы, пены и дымы.
Дисперсные системы изучаются в химии коллоидов. Известны жидкие, гелеподобные и твердые коллоиды.
В термодинамике существуют такие понятия, как изолированная, открытая и стабильная системы, а также моновариантная, бивариантная и поливариантная системы.
Изолированная система - система, которая не может обмениваться энергией и веществом с окружающей средой.
Открытая система обменивается энергией и веществом со средой.
В стабильной химической системе между веществами, образующими систему, существует равновесие.
Моновариантная система - химическая система, в которой две фазы находятся в равновесии.
Нонвариантная химическая система - система, в которой три компонента (или фазы) находятся в равновесии.
Бивариантная (поливариантная) система - система, представляющая собой одну фазу и сумму трех или более независимых компонентов и внешних факторов (температура и давление).
Среди агрегированных состояний известны конденсированные состояния при стандартных условиях (Т =291,15 К; Р=101,325 кПа).
Конденсированные вещества могут находиться в твердом или жидком состояниях; твердые вещества могут быть кристаллическими или аморфными.
Стабильность химических систем достигается присутствием химических связей и взаимодействий, которые различаются по энергии и природе. В дисперсных системах имеют место наиболее разнообразные системы связей и взаимодействий.
Дисперсионная среда - вещество, которое присутствует протяженной фазой в дисперсной системе.
Дисперсная фаза - вещество, распределенное в среде.
В зависимости от линейных размеров дисперсионной фазы образуются гомогенные и гетерогенные дисперсные системы. Гомогенные дисперсные системы обычно называются растворами. Они могут быть твердыми, жидкими или газовыми. В растворах линейные размеры дисперсной фазы не превышают 1 нм. Гетерогенные дисперсные системы разделяются на коллоидные системы (линейный размер частиц более 100 нм). В зависимости от агрегатного состояния дисперсной среды различают твердые (сплавы); жидкие (пены, эмульсии, суспензии); газовые (туманы, дымы, аэрозоли, газовые смеси) дисперсные системы. В этих системах возможны два или более видов фазовых границ, а также два или более видов химических связей. В сплавах между фазами образуются граничные слои с переменной электронной плотностью. При образовании сплавов в основном принимают участие металлические связи, вместе с тем образование ионных и ковалентных связей также возможно.
Когда возникают пены, во взаимодействии участвуют газы и жидкие компоненты. В граничном слое обычно присутствует растворенный газ в соответствующей жидкости. Здесь главные химические связи ковалентные. Эмульсии содержат две или более жидких фаз, а суспензии имеют твердые и жидкие фазы (в суспензиях твердая фаза распределяется в жидкой среде).
Дымы являются дисперсными системами, в которых твердые частицы распределяются в газовой среде. В то же время в туманах частицы жидкой фазы распределяются в газовых смесях.
Во всех этих случаях присутствуют различные химические связи и взаимодействия, а также для соответствующих дисперсных систем наблюдается особенное распределение электронной плотности.
Известно, что молекулы химических веществ могут быть представлены в виде карт электронной плотности. При сложении такого описания целесообразно представлять химические системы в виде карт изменений плотности (или других свойств) для реальных фаз с учетом данных для межфазных слоев. Например, для суспензии, в которой распределены частицы практически одного размера и одной формы, имеющие на поверхности активные центры, взаимодействующие с дисперсионной средой, можно представить изменения плотности в одном направлении в виде диаграммы.
Поверхностный слой, образующийся на границе «суспензия - воздушная среда», обычно имеет большую, чем дисперсионная среда, плотность, поскольку химические частицы поверхностного слоя находятся под влиянием поля частиц во внутренних слоях дисперсионной среды и дисперсионной фазы. При этом не учитываются флуктуации плотности в дисперсионной среде и дисперсионной фазе. Для представления образования и свойств дисперсных систем являются важными такие понятия, как адсорбция, хемосорбция, адгезия, когезия, коагуляция, золь, гель, лиофобность, лиофильность.
Адсорбция - процесс увеличения концентрации химического соединения на межфазной поверхности по отношению к концентрации этого вещества в объеме.
Хемосорбция - адсорбция, сопровождающаяся химическими реакциями.
Процессы хемосорбции зачастую связываются (сопровождаются) процессами адгезии.
Адгезия - связывание различных жидких и твердых фаз на их границе.
Когезия - связывание (образование связей) между химическими частицами в гомогенной фазе.
Т.о., адгезия и когезия - противоположные процессы. Благодаря адгезии твердые тела могут быть изотропными и не разрушаться на отдельные фазы. Однако при определенных условиях возможны фазовые распределения или взаимодействия частиц дисперсной фазы между собой. Для коллоидных систем возможна коагуляция.
Коагуляция - слипание вместе частиц дисперсной фазы в коллоидных системах.
При коагуляции в жидкой дисперсной среде образуются гели.
Гели - желеподобные коллоидные системы с жидкой дисперсной средой.
Золи - обычно коллоидные растворы или коллоидные системы, включающие взаимодействующие между собой дисперсную фазу и дисперсную среду.
Для характеристики способности веществ к взаимодействию с жидкой средой применяют термины «лиофобность» и «лиофильность».
Основания (гидроксиды) – сложные вещества, молекулы которых в своём составе имеют одну или несколько гидрокси-групп OH. Чаще всего основания состоят из атома металла и группы OH. Например, NaOH – гидроксид натрия, Ca(OH) 2 – гидроксид кальция и др.
Существует основание – гидроксид аммония, в котором гидрокси-группа присоединена не к металлу, а к иону NH 4 + (катиону аммония). Гидроксид аммония образуется при растворении аммиака в воде (реакции присоединения воды к аммиаку):
NH 3 + H 2 O = NH 4 OH (гидроксид аммония).
Валентность гирокси-группы – 1. Число гидроксильных групп в молекуле основания зависит от валентности металла и равно ей. Например, NaOH, LiOH, Al (OH) 3 , Ca(OH) 2 , Fe(OH) 3 и т.д.
Все основания – твёрдые вещества, которые имеют различную окраску. Некоторые основания хорошо растворимы в воде (NaOH, KOH и др.). Однако большинство из них в воде не растворяются.
Растворимые в воде основания называются щелочами. Растворы щелочей «мыльные», скользкие на ощупь и довольно едкие. К щелочам относят гидроксиды щелочных и щелочноземельных металлов (KOH, LiOH, RbOH, NaOH, CsOH, Ca(OH) 2 , Sr(OH) 2 , Ba(OH) 2 и др.). Остальные являются нерастворимыми.
Нерастворимые основания – это амфотерные гидроксиды, которые при взаимодействии с кислотами выступают как основания, а со щёлочью ведут себя, как кислоты.
Разные основания отличаются разной способностью отщеплять гидрокси-группы, поэтому признаку они делятся на сильные и слабые основания.
Сильные основания в водных растворах легко отдают свои гидрокси-группы, а слабые – нет.
 Химические свойства оснований
Химические свойства оснований
Химические свойства оснований характеризуются отношением их к кислотам, ангидридам кислот и солям.
1. Действуют на индикаторы . Индикаторы меняют свою окраску в зависимости от взаимодействия с разными химическими веществами. В нейтральных растворах – они имеют одну окраску, в растворах кислот – другую. При взаимодействии с основаниями они меняют свою окраску: индикатор метиловый оранжевый окрашивается в жёлтый цвет, индикатор лакмус – в синий цвет, а фенолфталеин становится цвета фуксии.
2. Взаимодействуют с кислотными оксидами с образованием соли и воды:
2NaOH + SiO 2 → Na 2 SiO 3 + H 2 O.
3. Вступают в реакцию с кислотами, образуя соль и воду. Реакция взаимодействия основания с кислотой называется реакцией нейтрализации, так как после её окончания среда становится нейтральной:
2KOH + H 2 SO 4 → K 2 SO 4 + 2H 2 O.
4. Реагируют с солями, образуя новые соль и основание:
2NaOH + CuSO 4 → Cu(OH) 2 + Na 2 SO 4.
5. Способны при нагревании разлагаться на воду и основной оксид:
Cu(OH) 2 = CuO + H 2 O.
Остались вопросы? Хотите знать больше об основаниях?
Чтобы получить помощь репетитора – зарегистрируйтесь .
Первый урок – бесплатно!
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
 Классификация веществ Все вещества можно разделить на простые состоящие из атомов одного элемента и сложные – состоящие из атомов различных элементов. Простые вещества делятся на металлы и неметаллы: Металлы – s и d элементы. Неметаллы – p элементы. Сложные вещества делятся на органические и неорганические.
Классификация веществ Все вещества можно разделить на простые состоящие из атомов одного элемента и сложные – состоящие из атомов различных элементов. Простые вещества делятся на металлы и неметаллы: Металлы – s и d элементы. Неметаллы – p элементы. Сложные вещества делятся на органические и неорганические.
 Свойства металлов определяются способностью атомов отдавать свои электроны. Характерный тип химической связи для металлов – металлическая связь. Она характеризуется такими физическими свойствами: ковкость, тягучесть, теплопроводность, электропроводность. При комнатных условиях все металлы кроме ртути находятся в твердом состоянии.
Свойства металлов определяются способностью атомов отдавать свои электроны. Характерный тип химической связи для металлов – металлическая связь. Она характеризуется такими физическими свойствами: ковкость, тягучесть, теплопроводность, электропроводность. При комнатных условиях все металлы кроме ртути находятся в твердом состоянии.
 Свойства неметаллов определяются способностью атомов легко принимать электроны и плохо отдавать свои. Неметаллы обладают противоположными металлам физическими свойствами: их кристаллы хрупкие, отсутствует «металлический» блеск, низкие значения теплои электропроводности. Часть неметаллов при комнатных условиях газообразна.
Свойства неметаллов определяются способностью атомов легко принимать электроны и плохо отдавать свои. Неметаллы обладают противоположными металлам физическими свойствами: их кристаллы хрупкие, отсутствует «металлический» блеск, низкие значения теплои электропроводности. Часть неметаллов при комнатных условиях газообразна.

 Классификация органических соединений. По строению углеродного скелета: Насыщенные/ненасыщенные Линейные/разветвленные/циклические По наличию функциональных групп: Спирты Кислоты Простые и сложные эфиры Углеводы Альдегиды и кетоны
Классификация органических соединений. По строению углеродного скелета: Насыщенные/ненасыщенные Линейные/разветвленные/циклические По наличию функциональных групп: Спирты Кислоты Простые и сложные эфиры Углеводы Альдегиды и кетоны
 Оксиды – сложные вещества, молекулы которых состоят из двух элементов, один из которых – кислород в степени окисления -2. Оксиды делятся на солеобразующие и несолеобразующие(безразличные). Солеобразующие оксиды делятся на основные, кислотные и амфотерные.
Оксиды – сложные вещества, молекулы которых состоят из двух элементов, один из которых – кислород в степени окисления -2. Оксиды делятся на солеобразующие и несолеобразующие(безразличные). Солеобразующие оксиды делятся на основные, кислотные и амфотерные.
 Основные оксиды – это оксиды, образующие в реакциях с кислотами или кислотными оксидами соли. Основные оксиды образуются металлами с невысокой степенью окисления (+1, +2) – это элементы 1 й и 2 й групп периодической таблицы. Примеры основных оксидов: Na 2 O, Ca. O, Mg. O, Cu. O. Примеры реакций образования солей: Cu. O + 2 HCl Cu. Cl 2 + H 2 O, Mg. O + CO 2 Mg. CO 3.
Основные оксиды – это оксиды, образующие в реакциях с кислотами или кислотными оксидами соли. Основные оксиды образуются металлами с невысокой степенью окисления (+1, +2) – это элементы 1 й и 2 й групп периодической таблицы. Примеры основных оксидов: Na 2 O, Ca. O, Mg. O, Cu. O. Примеры реакций образования солей: Cu. O + 2 HCl Cu. Cl 2 + H 2 O, Mg. O + CO 2 Mg. CO 3.
 Основные оксиды Оксиды щелочных и щелочноземельных металлов реагируют с водой, образуя основания: Na 2 O + H 2 O 2 Na. OH Ca. O + H 2 O Ca(OH)2 Оксиды других металлов с водой не реагируют, соответствующие основания получаются косвенным путем.
Основные оксиды Оксиды щелочных и щелочноземельных металлов реагируют с водой, образуя основания: Na 2 O + H 2 O 2 Na. OH Ca. O + H 2 O Ca(OH)2 Оксиды других металлов с водой не реагируют, соответствующие основания получаются косвенным путем.
 Кислотные оксиды – это оксиды, образующие в реакциях с основаниями или с основными оксидами соли. Кислотные оксиды образуются элементами – неметаллами и d – элементами в высоких степенях окисления (+5, +6, +7). Примеры кислотных оксидов: N 2 O 5, SO 3, CO 2, Cr. O 3, V 2 O 5. Примеры реакций кислотных оксидов: SO 3 + 2 KOH K 2 SO 4 + H 2 O Ca. O + CO 2 Ca. CO 3
Кислотные оксиды – это оксиды, образующие в реакциях с основаниями или с основными оксидами соли. Кислотные оксиды образуются элементами – неметаллами и d – элементами в высоких степенях окисления (+5, +6, +7). Примеры кислотных оксидов: N 2 O 5, SO 3, CO 2, Cr. O 3, V 2 O 5. Примеры реакций кислотных оксидов: SO 3 + 2 KOH K 2 SO 4 + H 2 O Ca. O + CO 2 Ca. CO 3
 Кислотные оксиды Часть кислотных оксидов реагирует с водой с образованием соответствующих кислот: SO 3 + H 2 O H 2 SO 4 N 2 O 5 + H 2 O 2 HNO 3 Другие кислотные оксиды напрямую с водой не реагируют (Si. O 2 , Te. O 3 , Mo. O 3 , WO 3), соответствующие кислоты получаются косвенным путем. Один из способов получения кислотных оксидов – отнятие воды от соответствующих кислот. Поэтому кислотные оксиды иногда называются «ангидридами» .
Кислотные оксиды Часть кислотных оксидов реагирует с водой с образованием соответствующих кислот: SO 3 + H 2 O H 2 SO 4 N 2 O 5 + H 2 O 2 HNO 3 Другие кислотные оксиды напрямую с водой не реагируют (Si. O 2 , Te. O 3 , Mo. O 3 , WO 3), соответствующие кислоты получаются косвенным путем. Один из способов получения кислотных оксидов – отнятие воды от соответствующих кислот. Поэтому кислотные оксиды иногда называются «ангидридами» .
 Амфотерные оксиды обладают свойствами и кислотных и основных оксидов. С сильными кислотами такие оксиды реагируют как основные, а с сильными основаниями как кислотные: Sn. O + H 2 SO 4 Sn. SO 4 + H 2 O Sn. O + 2 KOH + H 2 O K 2
Амфотерные оксиды обладают свойствами и кислотных и основных оксидов. С сильными кислотами такие оксиды реагируют как основные, а с сильными основаниями как кислотные: Sn. O + H 2 SO 4 Sn. SO 4 + H 2 O Sn. O + 2 KOH + H 2 O K 2
 Способы получения оксидов Окисление простых веществ: 4 Fe + 3 O 2 2 Fe 2 O 3, S + O 2 SO 2. Горение сложных веществ: CH 4 + 2 O 2 CO 2 + 2 H 2 O, 2 SO 2 + O 2 2 SO 3. Термическое разложение солей, оснований и кислот. Примеры соответственно: Ca. CO 3 Ca. O + CO 2, Cd(OH)2 Cd. O + H 2 O, H 2 SO 4 SO 3 + H 2 O.
Способы получения оксидов Окисление простых веществ: 4 Fe + 3 O 2 2 Fe 2 O 3, S + O 2 SO 2. Горение сложных веществ: CH 4 + 2 O 2 CO 2 + 2 H 2 O, 2 SO 2 + O 2 2 SO 3. Термическое разложение солей, оснований и кислот. Примеры соответственно: Ca. CO 3 Ca. O + CO 2, Cd(OH)2 Cd. O + H 2 O, H 2 SO 4 SO 3 + H 2 O.
 Номенклатура оксидов Название оксида строится по формуле «оксид + название элемента в родительном падеже» . Если элемент образует несколько оксидов, то после названия в скобках указывают степень окисления элемента. Например: CO – оксид углерода (II), CO 2 – оксид углерода (IV), Na 2 O – оксид натрия. Иногда вместо степени окисления в названии указывается число атомов кислорода: монооксид, диоксид, триокид и т. д.
Номенклатура оксидов Название оксида строится по формуле «оксид + название элемента в родительном падеже» . Если элемент образует несколько оксидов, то после названия в скобках указывают степень окисления элемента. Например: CO – оксид углерода (II), CO 2 – оксид углерода (IV), Na 2 O – оксид натрия. Иногда вместо степени окисления в названии указывается число атомов кислорода: монооксид, диоксид, триокид и т. д.
 Гидроксиды – соединения, содержащие в своем составе гидроксогруппу (-OH). В зависимости от прочности связей в ряду Э-O-H гидроксиды делятся на кислоты и основания: У кислот самая слабая связь O-H, поэтому при их диссоциации образуется Э-О- и H+. У оснований самая слабая связь Э-О, поэтому при диссоциации образуются Э+ и OH-. У амфотерных гидроксидов может быть разорвана любая из этих двух связей, в зависимости от природы вещества, с которым реагирует гидроксид.
Гидроксиды – соединения, содержащие в своем составе гидроксогруппу (-OH). В зависимости от прочности связей в ряду Э-O-H гидроксиды делятся на кислоты и основания: У кислот самая слабая связь O-H, поэтому при их диссоциации образуется Э-О- и H+. У оснований самая слабая связь Э-О, поэтому при диссоциации образуются Э+ и OH-. У амфотерных гидроксидов может быть разорвана любая из этих двух связей, в зависимости от природы вещества, с которым реагирует гидроксид.
 Кислоты Термин «кислота» в рамках теории электролитической диссоциации имеет следующее определение: Кислоты – это вещества, диссоциирующие в растворах с образованием катионов водорода и анионов кислотного остатка. HA H++AКислоты делятся на сильные и слабые (по способности к диссоциации), на одно-, двух-, и трехосновные (по количеству содержащихся атомов водорода) и на кислородсодержащие и бескислородные. Например: H 2 SO 4 – сильная, двухосновная, кислородсодержащая.
Кислоты Термин «кислота» в рамках теории электролитической диссоциации имеет следующее определение: Кислоты – это вещества, диссоциирующие в растворах с образованием катионов водорода и анионов кислотного остатка. HA H++AКислоты делятся на сильные и слабые (по способности к диссоциации), на одно-, двух-, и трехосновные (по количеству содержащихся атомов водорода) и на кислородсодержащие и бескислородные. Например: H 2 SO 4 – сильная, двухосновная, кислородсодержащая.
 Химические свойства кислот 1. Взаимодействие с основаниями с образованием соли и воды (реакция нейтрализации): H 2 SO 4 + Cu (OH)2 Cu. SO 4 + 2 H 2 O. 2. Взаимодействие с основными и амфотерными оксидами с образованием солей и воды: 2 HNO 3 + Mg. O Mg(NO 3)2 + H 2 O, H 2 SO 4 + Zn. O Zn. SO 4 + H 2 O.
Химические свойства кислот 1. Взаимодействие с основаниями с образованием соли и воды (реакция нейтрализации): H 2 SO 4 + Cu (OH)2 Cu. SO 4 + 2 H 2 O. 2. Взаимодействие с основными и амфотерными оксидами с образованием солей и воды: 2 HNO 3 + Mg. O Mg(NO 3)2 + H 2 O, H 2 SO 4 + Zn. O Zn. SO 4 + H 2 O.
 Химические свойства кислот 3. Взаимодействие с металлами. Металлы, стоящие в “Ряду напряжений” до водорода, вытесняют водород из растворов кислот (кроме азотной и концентрированной серной кислот); при этом образуется соль: Zn + 2 HCl Zn. Cl 2 + H 2 Металлы, находящиеся в “Ряду напряжений” после водорода, водород из растворов кислот не вытесняют Cu + 2 HCl ≠.
Химические свойства кислот 3. Взаимодействие с металлами. Металлы, стоящие в “Ряду напряжений” до водорода, вытесняют водород из растворов кислот (кроме азотной и концентрированной серной кислот); при этом образуется соль: Zn + 2 HCl Zn. Cl 2 + H 2 Металлы, находящиеся в “Ряду напряжений” после водорода, водород из растворов кислот не вытесняют Cu + 2 HCl ≠.
 Химические свойства кислот 4. Некоторые кислоты при нагревании разлагаются: H 2 Si. O 3 H 2 O + Si. O 2 5. Менее летучие кислоты вытесняют более летучие кислоты из их солей: H 2 SO 4 конц + Na. Clтв Na. HSO 4 + HCl 6. Более сильные кислоты вытесняют менее сильные кислоты из растворов их солей: 2 HCl + Na 2 CO 3 2 Na. Cl + H 2 O + CO 2
Химические свойства кислот 4. Некоторые кислоты при нагревании разлагаются: H 2 Si. O 3 H 2 O + Si. O 2 5. Менее летучие кислоты вытесняют более летучие кислоты из их солей: H 2 SO 4 конц + Na. Clтв Na. HSO 4 + HCl 6. Более сильные кислоты вытесняют менее сильные кислоты из растворов их солей: 2 HCl + Na 2 CO 3 2 Na. Cl + H 2 O + CO 2
 Номенклатура кислот Названия бескислородных кислот составляют, добавляя к корню русского названия кислотообразующего элемента (или к названию группы атомов, например, CN – циан, CNS – родан) суффикс «-о-» , окончание «водородная» и слово «кислота» . Например: HCl – хлороводородная кислота H 2 S – сероводородная кислота HCN – циановодородная кислота
Номенклатура кислот Названия бескислородных кислот составляют, добавляя к корню русского названия кислотообразующего элемента (или к названию группы атомов, например, CN – циан, CNS – родан) суффикс «-о-» , окончание «водородная» и слово «кислота» . Например: HCl – хлороводородная кислота H 2 S – сероводородная кислота HCN – циановодородная кислота
 Номенклатура кислот Названия кислородсодержащих кислот образуются по формуле «название элемента» + «окончание» + «кислота» . Окончание меняется в зависимости от степени окисления кислотообразующего элемента. Окончания «–овая» / «-ная» используются для высших степеней окисления. HCl. O 4 – хлорная кислота. Затем используются окончание «–оватая» . HCl. O 3 – хлорноватая кислота. Затем используется окончание «–истая» . HCl. O 2 – хлористая кислота. Наконец, последнее окончание «-оватистая» HCl. O – хлорноватистая кислота.
Номенклатура кислот Названия кислородсодержащих кислот образуются по формуле «название элемента» + «окончание» + «кислота» . Окончание меняется в зависимости от степени окисления кислотообразующего элемента. Окончания «–овая» / «-ная» используются для высших степеней окисления. HCl. O 4 – хлорная кислота. Затем используются окончание «–оватая» . HCl. O 3 – хлорноватая кислота. Затем используется окончание «–истая» . HCl. O 2 – хлористая кислота. Наконец, последнее окончание «-оватистая» HCl. O – хлорноватистая кислота.
 Номенклатура кислот Если элемент образует всего две кислородсодержащие кислоты (например сера), то для высшей степени окисления используется окончание «–овая» / «- ная» , а для более низкой окончание «-истая» . Пример для кислот серы: H 2 SO 4 – серная кислота H 2 SO 3 – сернистая кислота
Номенклатура кислот Если элемент образует всего две кислородсодержащие кислоты (например сера), то для высшей степени окисления используется окончание «–овая» / «- ная» , а для более низкой окончание «-истая» . Пример для кислот серы: H 2 SO 4 – серная кислота H 2 SO 3 – сернистая кислота
 Номенклатура кислот Если один кислотный оксид присоединяет различное количество молекул воды при образовании кислоты, то кислота, содержащая большее количество воды обозначается приставкой «орто-» , а меньшее «мета-» . P 2 O 5 + H 2 O 2 HPO 3 - метафосфорная кислота P 2 O 5 + 3 H 2 O 2 H 3 PO 4 - ортофосфорная кислота.
Номенклатура кислот Если один кислотный оксид присоединяет различное количество молекул воды при образовании кислоты, то кислота, содержащая большее количество воды обозначается приставкой «орто-» , а меньшее «мета-» . P 2 O 5 + H 2 O 2 HPO 3 - метафосфорная кислота P 2 O 5 + 3 H 2 O 2 H 3 PO 4 - ортофосфорная кислота.
 Основания Термин «основание» в рамках теории электролитической диссоциации имеет следующее определение: Основаниями – это вещества, диссоциирующие в растворах с образованием гидроксид - ионов (OH‾) и ионов металлов. Основания классифицируются на слабые и сильные(по способности к диссоциации), на одно-, двух-, трехкислотные (по количеству гидроксогрупп, которые могут заместиться на кислотный остаток) на растворимые (щелочи) и нерастворимые(по способности растворяться в воде). Например, KOH – сильное, однокислотное, растворимое.
Основания Термин «основание» в рамках теории электролитической диссоциации имеет следующее определение: Основаниями – это вещества, диссоциирующие в растворах с образованием гидроксид - ионов (OH‾) и ионов металлов. Основания классифицируются на слабые и сильные(по способности к диссоциации), на одно-, двух-, трехкислотные (по количеству гидроксогрупп, которые могут заместиться на кислотный остаток) на растворимые (щелочи) и нерастворимые(по способности растворяться в воде). Например, KOH – сильное, однокислотное, растворимое.
 Химические свойства оснований 1. Взаимодействие с кислотами: Ca(OH)2 + H 2 SO 4 Ca. SO 4 + H 2 O 2. Взаимодействие с кислотными оксидами: Ca(OH)2 + CO 2 Ca. CO 3 + H 2 O 3. Взаимодействие с амфотерными оксидами: 2 KOH + Sn. O + H 2 O K 2
Химические свойства оснований 1. Взаимодействие с кислотами: Ca(OH)2 + H 2 SO 4 Ca. SO 4 + H 2 O 2. Взаимодействие с кислотными оксидами: Ca(OH)2 + CO 2 Ca. CO 3 + H 2 O 3. Взаимодействие с амфотерными оксидами: 2 KOH + Sn. O + H 2 O K 2
 Химические свойства оснований 4. Взаимодействие с амфотерными основаниями: 2 Na. OH + Zn(OH)2 Na 2 5. Термическое разложение оснований с образованием оксидов и воды: Ca(OH)2 Ca. O + H 2 O. Гидроксиды щелочных металлов при нагревании не распадаются. 6. Взаимодействие с амфотерными металлами (Zn, Al, Pb, Sn, Be): Zn + 2 Na. OH + 2 H 2 O Na 2 + H 2
Химические свойства оснований 4. Взаимодействие с амфотерными основаниями: 2 Na. OH + Zn(OH)2 Na 2 5. Термическое разложение оснований с образованием оксидов и воды: Ca(OH)2 Ca. O + H 2 O. Гидроксиды щелочных металлов при нагревании не распадаются. 6. Взаимодействие с амфотерными металлами (Zn, Al, Pb, Sn, Be): Zn + 2 Na. OH + 2 H 2 O Na 2 + H 2
 Номенклатура оснований Название основания образуется по формуле «гидроксид» + «название металла в родительном падеже» . Если элемент образует несколько гидроксидов, то в скобках указывается его степень окисления. Например Cr(OH)2 – гидроксид хрома (II), Cr(OH)3 – гидроксид хрома (III). Иногда в названии приставкой к слову «гидроксид» указывается количество гидроксогрупп – моногидроксид, дигидроксид, тригидроксид, и т. д.
Номенклатура оснований Название основания образуется по формуле «гидроксид» + «название металла в родительном падеже» . Если элемент образует несколько гидроксидов, то в скобках указывается его степень окисления. Например Cr(OH)2 – гидроксид хрома (II), Cr(OH)3 – гидроксид хрома (III). Иногда в названии приставкой к слову «гидроксид» указывается количество гидроксогрупп – моногидроксид, дигидроксид, тригидроксид, и т. д.
 Соли Термин «основание» в рамках теории электролитической диссоциации имеет следующее определение: Соли - это вещества, диссоциирующие в растворах или в расплавах с образованием положительно заряженных ионов, отличных от ионов водорода, и отрицательно заряженных ионов, отличных от гидроксид – ионов. Соли рассматриваются как продукт частичного или полного замещения атомов водорода на атомы металла или гидроксогрупп на кислотный остаток. Если замещение происходит полностью, то образуется нормальная (средняя) соль. Если замещение происходит частично, то такие соли называются кислыми(имеются атомы водорода), либо основными (имеются гидроксогруппы).
Соли Термин «основание» в рамках теории электролитической диссоциации имеет следующее определение: Соли - это вещества, диссоциирующие в растворах или в расплавах с образованием положительно заряженных ионов, отличных от ионов водорода, и отрицательно заряженных ионов, отличных от гидроксид – ионов. Соли рассматриваются как продукт частичного или полного замещения атомов водорода на атомы металла или гидроксогрупп на кислотный остаток. Если замещение происходит полностью, то образуется нормальная (средняя) соль. Если замещение происходит частично, то такие соли называются кислыми(имеются атомы водорода), либо основными (имеются гидроксогруппы).
 Химические свойства солей 1. Соли вступают в реакции ионного обмена, если при этом образуется осадок, слабый электролит или выделяется газ: с щелочами реагируют соли, катионам металлов которых соответствуют нерастворимые основания: Cu. SO 4 + 2 Na. OH Na 2 SO 4 + Cu (OH)2↓ с кислотами взаимодействуют соли: а) катионы которых образуют с анионом новой кислоты нерастворимую соль: Ba. Cl 2 + H 2 SO 4 Ba. SO 4↓ + 2 HCl б) анионы которой отвечают неустойчивой угольной или какойлибо летучей кислоте (в последнем случае реакция проводится между твердой солью и концентрированной кислотой): Na 2 CO 3 + 2 HCl 2 Na. Cl + H 2 O + CO 2, Na. Clтв + H 2 SO 4 конц Na. HSO 4 + HCl;
Химические свойства солей 1. Соли вступают в реакции ионного обмена, если при этом образуется осадок, слабый электролит или выделяется газ: с щелочами реагируют соли, катионам металлов которых соответствуют нерастворимые основания: Cu. SO 4 + 2 Na. OH Na 2 SO 4 + Cu (OH)2↓ с кислотами взаимодействуют соли: а) катионы которых образуют с анионом новой кислоты нерастворимую соль: Ba. Cl 2 + H 2 SO 4 Ba. SO 4↓ + 2 HCl б) анионы которой отвечают неустойчивой угольной или какойлибо летучей кислоте (в последнем случае реакция проводится между твердой солью и концентрированной кислотой): Na 2 CO 3 + 2 HCl 2 Na. Cl + H 2 O + CO 2, Na. Clтв + H 2 SO 4 конц Na. HSO 4 + HCl;
 Химические свойства солей в) анионы которой отвечают малорастворимой кислоте: Na 2 Si. O 3 + 2 HCl H 2 Si. O 3↓ + 2 Na. Cl г) анионы которой отвечают слабой кислоте: 2 CH 3 COONa + H 2 SO 4 Na 2 SO 4 + 2 CH 3 COOH 2. cоли взаимодействуют между собой, если одна из образующихся новых солей нерастворима или разлагается (полностью гидролизуется) с выделением газа или осадка: Ag. NO 3 + Na. Cl Na. NO 3+ Ag. Cl↓ 2 Al. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O 2 Al (OH)3↓ + 6 Na. Cl + 3 CO 2
Химические свойства солей в) анионы которой отвечают малорастворимой кислоте: Na 2 Si. O 3 + 2 HCl H 2 Si. O 3↓ + 2 Na. Cl г) анионы которой отвечают слабой кислоте: 2 CH 3 COONa + H 2 SO 4 Na 2 SO 4 + 2 CH 3 COOH 2. cоли взаимодействуют между собой, если одна из образующихся новых солей нерастворима или разлагается (полностью гидролизуется) с выделением газа или осадка: Ag. NO 3 + Na. Cl Na. NO 3+ Ag. Cl↓ 2 Al. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O 2 Al (OH)3↓ + 6 Na. Cl + 3 CO 2
 Химические свойства солей 3. Соли могут вступать во взаимодействие с металлами, если металл, которому соответствует катион соли, находится в“Ряду напряжений “правее реагирующего свободного металла (более активный металл вытесняет менее активный металл из раствора его соли): Zn + Cu. SO 4 Zn. SO 4 + Cu 4. Некоторые соли разлагаются при нагревании: Ca. CO 3 Ca. O + CO 2 5. Некоторые соли способны реагировать с водой и образовывать кристаллогидраты: Cu. SO 4 + 5 H 2 O Cu. SO 4*5 H 2 O
Химические свойства солей 3. Соли могут вступать во взаимодействие с металлами, если металл, которому соответствует катион соли, находится в“Ряду напряжений “правее реагирующего свободного металла (более активный металл вытесняет менее активный металл из раствора его соли): Zn + Cu. SO 4 Zn. SO 4 + Cu 4. Некоторые соли разлагаются при нагревании: Ca. CO 3 Ca. O + CO 2 5. Некоторые соли способны реагировать с водой и образовывать кристаллогидраты: Cu. SO 4 + 5 H 2 O Cu. SO 4*5 H 2 O
 Химические свойства солей 6. Соли подвергаются гидролизу. Подробно этот процесс будет рассмотрен в дальнейших лекциях. 7. Химические свойства кислых и основных солей отличаются от свойств средних солей тем, что кислые соли вступают также во все реакции, характерные для кислот, а основные соли вступают во все реакции, характерные для оснований. Например: Na. HSO 4 + Na. OH Na 2 SO 4 + H 2 O, Mg. OHCl + HCl Mg. Cl 2 + H 2 O.
Химические свойства солей 6. Соли подвергаются гидролизу. Подробно этот процесс будет рассмотрен в дальнейших лекциях. 7. Химические свойства кислых и основных солей отличаются от свойств средних солей тем, что кислые соли вступают также во все реакции, характерные для кислот, а основные соли вступают во все реакции, характерные для оснований. Например: Na. HSO 4 + Na. OH Na 2 SO 4 + H 2 O, Mg. OHCl + HCl Mg. Cl 2 + H 2 O.
 Получение солей 1. Взаимодействие основного оксида с кислотой: Cu. O + H 2 SO 4 Cu. SO 4 + H 2 O 2. Взаимодействие металла с солью другого металла: Mg + Zn. Cl 2 Mg. Cl 2 + Zn 3. Взаимодействие металла с кислотой: Mg + 2 HCl Mg. Cl 2 + H 2 4. Взаимодействие основания с кислотным оксидом: Ca(OH)2 + CO 2 Ca. CO 3 + H 2 O 5. Взаимодействие основания с кислотой: Fe(OH)3 + 3 HCl Fe. Cl 3 + 3 H 2 O
Получение солей 1. Взаимодействие основного оксида с кислотой: Cu. O + H 2 SO 4 Cu. SO 4 + H 2 O 2. Взаимодействие металла с солью другого металла: Mg + Zn. Cl 2 Mg. Cl 2 + Zn 3. Взаимодействие металла с кислотой: Mg + 2 HCl Mg. Cl 2 + H 2 4. Взаимодействие основания с кислотным оксидом: Ca(OH)2 + CO 2 Ca. CO 3 + H 2 O 5. Взаимодействие основания с кислотой: Fe(OH)3 + 3 HCl Fe. Cl 3 + 3 H 2 O
 Получение солей 6. Взаимодействие соли с основанием: Fe. Cl 2 + 2 KOH Fe(OH)2 + 2 KCl 7. Взаимодействие двух солей: Ba(NO 3)2 + K 2 SO 4 Ba. SO 4 + 2 KNO 3 8. Взаимодействие металла с неметаллом: 2 K + S K 2 S 9. Взаимодействие кислоты с солью: Ca. CO 3 + 2 HCl Ca. Cl 2 + H 2 O + CO 2 10. Взаимодействие кислотного и основного оксидов: Ca. O + CO 2 Ca. CO 3
Получение солей 6. Взаимодействие соли с основанием: Fe. Cl 2 + 2 KOH Fe(OH)2 + 2 KCl 7. Взаимодействие двух солей: Ba(NO 3)2 + K 2 SO 4 Ba. SO 4 + 2 KNO 3 8. Взаимодействие металла с неметаллом: 2 K + S K 2 S 9. Взаимодействие кислоты с солью: Ca. CO 3 + 2 HCl Ca. Cl 2 + H 2 O + CO 2 10. Взаимодействие кислотного и основного оксидов: Ca. O + CO 2 Ca. CO 3
 Номенклатура солей Название средней соли формируется по следующему правилу: «название кислотного остатка в именительном падеже» + «название металла в родительном падеже» . Если металл может входить в состав соли в нескольких степенях окисления, то степень окисления указывается в скобках после названия соли.
Номенклатура солей Название средней соли формируется по следующему правилу: «название кислотного остатка в именительном падеже» + «название металла в родительном падеже» . Если металл может входить в состав соли в нескольких степенях окисления, то степень окисления указывается в скобках после названия соли.
 Названия кислотных остатков. Для бескислородных кислот название кислотного остатка состоит из корня латинского названия элемента и окончания «ид» . Например: Na 2 S- сульфид натрия, Na. Cl – хлорид натрия. Для кислородсодержащих кислот название остатка состоит из корня латинского названия и нескольких вариантов окончаний.
Названия кислотных остатков. Для бескислородных кислот название кислотного остатка состоит из корня латинского названия элемента и окончания «ид» . Например: Na 2 S- сульфид натрия, Na. Cl – хлорид натрия. Для кислородсодержащих кислот название остатка состоит из корня латинского названия и нескольких вариантов окончаний.
 Названия кислотных остатков. Для кислотного остатка с элементов в высшей степени окисления используется окончание «ат» . Na 2 SO 4 – сульфат натрия. Для кислотного остатка с меньшей степенью окисления (-истая кислота) используется окончание «-ит» . Na 2 SO 3 – сульфит натрия. Для кислотного остатка с еще меньшей степенью окисления (-оватистая кислота) используется приставка «гиппо-» и окончание «-ит» . Na. Cl. O – гиппохлорит натрия.
Названия кислотных остатков. Для кислотного остатка с элементов в высшей степени окисления используется окончание «ат» . Na 2 SO 4 – сульфат натрия. Для кислотного остатка с меньшей степенью окисления (-истая кислота) используется окончание «-ит» . Na 2 SO 3 – сульфит натрия. Для кислотного остатка с еще меньшей степенью окисления (-оватистая кислота) используется приставка «гиппо-» и окончание «-ит» . Na. Cl. O – гиппохлорит натрия.
 Названия кислотных остатков. Некоторые кислотные остатки называются историческими названиями Na. Cl. O 4 – перхлорат натрия. К названию кислых солей добавляется приставка «гидро» , и перед ней еще одна приставка, указывающая на число незамещенных (оставшихся) атомов водорода. Например, Na. H 2 PO 4 – дигидроортофосфат натрия. Аналогично к названию металла основных солей добавляется приставка «гидроксо-» . Например, Cr(OH)2 NO 3 – нитрат дигидроксохрома (III).
Названия кислотных остатков. Некоторые кислотные остатки называются историческими названиями Na. Cl. O 4 – перхлорат натрия. К названию кислых солей добавляется приставка «гидро» , и перед ней еще одна приставка, указывающая на число незамещенных (оставшихся) атомов водорода. Например, Na. H 2 PO 4 – дигидроортофосфат натрия. Аналогично к названию металла основных солей добавляется приставка «гидроксо-» . Например, Cr(OH)2 NO 3 – нитрат дигидроксохрома (III).
 Названия и формулы кислот и их остатков Формула кислоты Кислотный остаток Название кислотного остатка 2 3 4 Азотная HNO 3 ‾ нитрат Азотистая HNO 2 ‾ нитрит Бромоводородная HBr Br ‾ бромид Йодоводородная HI I‾ йодид Кремниевая H 2 Si. O 32¯ силикат Марганцовая HMn. O 4¯ перманганат Марганцовистая H 2 Mn. O 42¯ манганат Метафосфорная HPO 3¯ H 3 As. O 43¯ Название кислоты 1 Мышьяковая метафосфат арсенат
Названия и формулы кислот и их остатков Формула кислоты Кислотный остаток Название кислотного остатка 2 3 4 Азотная HNO 3 ‾ нитрат Азотистая HNO 2 ‾ нитрит Бромоводородная HBr Br ‾ бромид Йодоводородная HI I‾ йодид Кремниевая H 2 Si. O 32¯ силикат Марганцовая HMn. O 4¯ перманганат Марганцовистая H 2 Mn. O 42¯ манганат Метафосфорная HPO 3¯ H 3 As. O 43¯ Название кислоты 1 Мышьяковая метафосфат арсенат
 Формула кислоты Мышьяковистая H 3 As. O 3 Ортофосфорная H 3 PO 4 Название кислоты Пирофосфорная H 4 P 2 O 7 Двухромовая Родановодородная Сернистая Фосфористая Фтороводородная (плавиковая) Хлороводородная (соляная) Хлорная Хлорноватая Хлористая Хлорноватистая Хромовая Циановодородная (синильная) H 2 Cr 2 O 7 HCNS H 2 SO 4 H 2 SO 3 H 3 PO 3 Кислотный Название кислотного остаток остатка As. O 33¯ арсенит PO 43¯ ортофосфат (фосфат) пирофосфат P 2 O 7 4 ¯ (дифосфат) Cr 2 O 72¯ дихромат CNS¯ роданид SO 42¯ сульфат SO 32¯ сульфит PO 33¯ фосфит HF F¯ HCl. O 4 HCl. O 3 HCl. O 2 HCl. O H 2 Cr. O 4 Cl¯ Cl. O 4¯ Cl. O 3¯ Cl. O 2¯ Cl. O¯ Cr. O 42¯ HCN CN¯ фторид хлорид перхлорат хлорит гипохлорит хромат цианид
Формула кислоты Мышьяковистая H 3 As. O 3 Ортофосфорная H 3 PO 4 Название кислоты Пирофосфорная H 4 P 2 O 7 Двухромовая Родановодородная Сернистая Фосфористая Фтороводородная (плавиковая) Хлороводородная (соляная) Хлорная Хлорноватая Хлористая Хлорноватистая Хромовая Циановодородная (синильная) H 2 Cr 2 O 7 HCNS H 2 SO 4 H 2 SO 3 H 3 PO 3 Кислотный Название кислотного остаток остатка As. O 33¯ арсенит PO 43¯ ортофосфат (фосфат) пирофосфат P 2 O 7 4 ¯ (дифосфат) Cr 2 O 72¯ дихромат CNS¯ роданид SO 42¯ сульфат SO 32¯ сульфит PO 33¯ фосфит HF F¯ HCl. O 4 HCl. O 3 HCl. O 2 HCl. O H 2 Cr. O 4 Cl¯ Cl. O 4¯ Cl. O 3¯ Cl. O 2¯ Cl. O¯ Cr. O 42¯ HCN CN¯ фторид хлорид перхлорат хлорит гипохлорит хромат цианид
Химическая промышленность - вид промышленности, в котором ключевое значение имеет переработка сырья химическими методами. Основными материалами, использующимися в этой отрасли, являются различное минеральное сырьё и нефть. Роль химической промышленности в современном мире очень велика. Благодаря ей люди могут пользоваться различными пластмассовыми и пластиковыми изделиями, а также другими продуктами переработки нефти. Кроме этого, отрасль даёт взрывчатые вещества, удобрения для сельскохозяйственных нужд, лекарственные препараты и так далее.
Развитие

Началом истории этой отрасли принято считать промышленный переворот, который произошёл в начале XVII века. До XVI века «наука о веществах» вообще развивалась очень медленно, но, как только люди научились применять эти знания в промышленности, многое изменилось. Самым первым продуктом химической промышленности стала серная кислота, которая и сейчас остаётся исключительно важным веществом и используется во многих сферах деятельности человека. В то время это соединение в основном использовалось в обработке руд металлов, необходимых для промышленной революции в большом количестве. Первые предприятия по выпуску серной кислоты были созданы в Англии, Франции и России.
Вторым этапом развития этой сферы стала необходимость массового выпуска кальцинированной соды. Это вещество было необходимо для обеспечения производства стекла и тканей.

На первом этапе самый большой вклад в развитие отрасли внесла Англия. С увеличением интереса к органической химии всё большее влияние на развитие этой науки оказывала Германия, чьи учёные до сих пор считаются одними из лучших специалистов в этой сфере. В начале XX века большая часть химических производств находилась именно в этой стране, что, по мнению некоторых аналитиков, обеспечило немецким лидерам уверенность в победе в Первой мировой войне из-за высокого качества взрывчатых веществ и перспективных исследований химического оружия. Кстати, впервые боевой отравляющий газ применили именно германские войска.
Отрасли химической промышленности

Сейчас актуальна как неорганическая, так и органическая химия, ежегодно совершается множество открытий в этих сферах. Наиболее перспективными разработками являются:
- Переработка нефти.
- Создание лекарственных препаратов.
- Создание удобрений.
- Создание полимеров и пластмасс.
- Изучение проводниковых свойств веществ.
Над созданием идеального проводника учёные работают уже несколько десятилетий. В случае успеха человечество сможет использовать ресурсы планеты гораздо более эффективно.
Химическая промышленность в России

Нефтехимия

Нефтехимия - ключевая отрасль химической промышленности в России. Во многом это связано с исключительно важной ролью нефтеперерабатывающей промышленности в экономике страны. Учебные заведения ежегодно выпускают десятки тысяч специалистов-нефтехимиков. Государство также выделяет большие деньги на спонсирование исследований в этой области.
Ежегодный объём продаж всех нефтехимических производств составляет более 500 миллиардов рублей.
Производство аммиака

«Тольяттиазот» является одним из ведущих производителей аммиака в мире. С недавнего времени фирма выпускает более 3 миллионов тонн газа в год, это исключительно высокий показатель. По оценкам специалистов, доля этой компании в мировом производстве аммиака составляет от 8 до 10%, также предприятие занимается производством минеральных удобрений и занимает в этом секторе около 20% российского рынка.
Производство удобрений

Немаловажной частью отрасли является и производство удобрений. На территории России расположены очень крупные месторождения сырьевых ресурсов для этой отрасли. Производство ресурсов для создания химических удобрений также хорошо развито. Во времена СССР над повышением эффективности удобрений работали лучшие учёные, сделавшие немало фундаментальных открытий в этой области. Благодаря этому Россия является одним из важнейших экспортёров удобрений.
Фармакологическая промышленность

Производство лекарственных средств и их компонентов является очень перспективным направлением. В настоящее время эта отрасль не покрывает российских потребностей, а создание многих препаратов даже не налажено. Поэтому ежегодно иностранные инвесторы, включая крупные химические концерны, вкладывают средства на развитие этой отрасли. Тем не менее существенное увеличение объёмов производства и качества продукции, по оценкам аналитиков, произойдёт в лучшем случае через десять лет.
Химическая промышленность в мире

Наиболее развита химическая промышленность в Германии, Великобритании и США. То есть среди европейских стран наиболее продвинутыми обычно являются государства, которые внесли определённый вклад в развитие химии как науки. В случае с США это связано с благоприятными условиями для развития химии и фармакологии: хорошая экономическая обстановка, наличие больших сырьевых ресурсов и развитой транспортной системы, переманивание лучших специалистов из других стран.
В частности, в пятёрке концернов с наибольшей прибылью 2 компании из Германии, 2 из Великобритании и одна из США.
Недавно мы с друзьями смотрели довольно интересный фильм. В нем рассказывалось о нашем будущем, о том, что будет с жизнью людей. Вообще, как я поняла жанр этого фильма, был фантастика. И в одной из сцен говорилось о возрастании химической промышленности, и о том что вскоре мы не сможем полноценно жить, из-за того что весь мир будет окутан химическими материалами. Все, конечно, посмеялись и пустили этот момент вскользь, но я задумалась, что ведь действительно химическая промышленность постепенно продвигается на первый план, вытесняя другие сферы деятельности, и это меня немного насторожило. Я решила во всем разобраться и теперь хочу рассказать и вам.
Что такое химическая промышленность
Химическая промышленность – исключительная деятельность в экономике , основой которой служит процесс химизации , т.е. использования химических способов, материалов и процессов в различные отрасли сфер хозяйства.
Она выделяется непростой организацией, включающей данные отрасли:
- добычу горно-химического сырья;
- основную химию;
- химию полимеров (органический синтез).

Даже по объяснению данного термина я уже сделала вывод о значимости данной промышленности, и эта значимость бесконечно огромна. Ведь химическая промышленность включает возможность потребления сырья и утилизацию почти всех отходов производства, даже самых токсичных. На мой взгляд, это очень весомый аргумент о роли данной деятельности в промышленном мире. Ни одна отрасль не может сравниться с хим. промышленностью в производстве фактически новых материалов с заранее заданными свойствами.

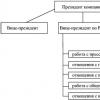
Факторы размещения предприятий химической промышленности
В основном к факторам размещения относится:
- сырьевой фактор;
- потребительский фактор;
- потребительски-сырьевой фактор.
Специфика размещения данных производств в России – концентрация в европейской части страны. Эту особенность обуславливает несколько причин. Среди главных – близость потребителя и наличие сырья (потребительски-сырьевой фактор ).

Примеры размещения
В основном, конечно добычу сырья можно отнести к сырьевому фактору. К примеру, горно-химические предприятия располагаются в Березниках и Соликамске, потому что здесь находится одно из крупнейших месторождений калийных солей. Фосфорные удобрения вырабатывают из апатитов, добываемых в Хибинах.Тем не менее, самым важным фактором химических предприятий является потребительский фактор . Практически все центры расположены в крупных городах. Например, какое либо предприятие удобней построить в Санкт-Петербурге, где проживает много людей и есть спрос, нежели чем в провинциальном городке с небольшим населением.